
کهکشان راه شیمی
نوشتن بیرون جهیدن از صف مردگان است.
کهکشان راه شیمی
نوشتن بیرون جهیدن از صف مردگان است.درباره من
پیوندها
- معرفی رشته های دانشگاهی
- موتور PDF
- دبیرستان فرزانگان تهران
- دبیرستان علامه حلی تهران
- دبیرستان علامه مشهد
- خانه شیمی دکتر محمد
- اداره چاپ کتب درسی
- مدرسه مجازی ایرانیان
- شبکه آموزش لیدیس
- خلاقیت
- آمار به روز جهان
- شبکه فیزیک هوپا
- موتور جستجوی شیمی
- جدول تناوبی عناصر
- شیمی دبیرستان
- کنکور
- دبیرستانی کنکوری
- داده های زمین شناسی
- پاورپوینت شیمی
- آموزش الکترونیکی رشد
- آموزش رایگان کنکور
- قانون هس
- آموزش شیمی یک
- فایل فلاش
- آموزش شیمی
- دهکده آموزش شیمی
- انیمیشن و عکس شیمی
- آّموزش شیمی دو
- آموزش شیمی یک
- بازی شیمی
- پاور پوینت شیمی
- جدول تناوبی فارسی
- شیمی نوین
- پاور پوینت شیمی
- انتشار گاز کربنیک
- بازی با فیزیک
- کنکور مشرقی
- محمد گنجی
- آموزش شیمی یک
- بازی شیمی
- بازی شیمی
- جدول ایزوتوپهای عناصر
- آموزش ویدیویی
- شیمیدان
- شیمی دبیرستان
- شیمی دبیرستان
- دبیرستان ماندگار البرز تهران
- انیمیشن
- شریف شیمی
- کلاس شیمی
- شیمی
- انجمن معلمان ایران
- سایت آموزشی کاشیها
- دیکشنری شیمی
- وب منیژه خواجه پور
- درمانگاه شیمی
- مهدی ضمیری
- مجله شیمیدان
- این جیه؟
- آموزش شیمی
- شیمی زنده
- sigmaaldrich
- آموزش شیمی یک رشد
- موتور جستجوی شیمی
- پایگاه موازته ی واکنش های شیمیایی
- ثبت اختراع آمریکا
- pubchem
- تمرین نامگذاری آلکان شاخه دار
- کتاب طلایی آیوپاک
- رسم آنلاین ساختار مولکول
- رسم آنلاین ساختار مولکول آلی
- رسم آنلاین ساختار مولکول
- نمای سه بعدی جامدات کووالانسی
- کتاب های شیمی قدیمی
- اندازه واقعی کشورها
- Mineralogy Database
جدیدترین یادداشتها
همه- آمادگی برای کنکور 1404
- تحلیل شیمیایی مرگ اسکندر مقدونی
- در حاشیه تصحیح پاسخبرگ های آزمون نهایی خرداد ماه 1404 شیمی دوازدهم و رسیدگی به اعتراضات
- آخرین وعده ی آلبرت
- اتانول یا متانول، مساله اینست
- خطر دستگاه تصفیه آب
- ضرر یک جستوجوی ساده
- بنزین سبز ایرانی
- پرنده ی گوزو
- پایان بشر
- و باز هم خطر هوش مصنوعی
- آغاز بیگبنگ معکوس
- کنکور 1405
- رویای تبدیل کربن دی اکسید به سیمان
- خروج خانواده های افغان از مرز دوغارون
بایگانی
- تیر 1404 64
- خرداد 1404 59
- اردیبهشت 1404 92
- فروردین 1404 112
- اسفند 1403 42
- بهمن 1403 23
- دی 1403 50
- آذر 1403 72
- آبان 1403 56
- مهر 1403 38
- شهریور 1403 29
- مرداد 1403 37
- تیر 1403 21
- خرداد 1403 49
- اردیبهشت 1403 61
- فروردین 1403 74
- اسفند 1402 83
- بهمن 1402 105
- دی 1402 122
- آذر 1402 45
- آبان 1402 62
- مهر 1402 62
- شهریور 1402 22
- مرداد 1402 14
- تیر 1402 32
- خرداد 1402 26
- اردیبهشت 1402 17
- فروردین 1402 51
- اسفند 1401 66
- بهمن 1401 38
- دی 1401 37
- آذر 1401 17
- آبان 1401 45
- مهر 1401 15
- شهریور 1401 29
- مرداد 1401 20
- تیر 1401 30
- خرداد 1401 44
- اردیبهشت 1401 57
- فروردین 1401 50
- اسفند 1400 33
- بهمن 1400 45
- دی 1400 19
- آذر 1400 26
- آبان 1400 32
- مهر 1400 37
- شهریور 1400 41
- مرداد 1400 20
- تیر 1400 24
- خرداد 1400 15
- اردیبهشت 1400 20
- فروردین 1400 25
- اسفند 1399 19
- بهمن 1399 13
- دی 1399 7
- آذر 1399 20
- آبان 1399 40
- مهر 1399 64
- شهریور 1399 26
- مرداد 1399 111
- تیر 1399 71
- خرداد 1399 29
- اردیبهشت 1399 40
- فروردین 1399 54
- اسفند 1398 35
- بهمن 1398 45
- دی 1398 23
- آذر 1398 28
- آبان 1398 14
- مهر 1398 18
- شهریور 1398 57
- مرداد 1398 41
- تیر 1398 21
- خرداد 1398 2
- دی 1397 2
- خرداد 1397 1
- اردیبهشت 1397 2
- اسفند 1396 1
- بهمن 1396 1
- دی 1396 1
- آبان 1396 4
- اردیبهشت 1396 1
- دی 1395 3
- خرداد 1395 1
- اردیبهشت 1395 1
- دی 1394 1
- آذر 1394 2
- تیر 1394 3
- خرداد 1394 11
- اردیبهشت 1394 3
- فروردین 1394 9
- اسفند 1393 19
- بهمن 1393 14
- دی 1393 4
- آذر 1393 18
- آبان 1393 22
- مهر 1393 9
- شهریور 1393 3
- مرداد 1393 10
- تیر 1393 7
- خرداد 1393 5
- اردیبهشت 1393 6
- فروردین 1393 1
- اسفند 1392 1
- بهمن 1392 8
- دی 1392 1
- آذر 1392 5
- آبان 1392 15
- مهر 1392 4
- شهریور 1392 10
- مرداد 1392 18
- تیر 1392 3
- خرداد 1392 3
- اردیبهشت 1392 8
- فروردین 1392 10
- اسفند 1391 11
- بهمن 1391 9
- دی 1391 7
- آذر 1391 6
- آبان 1391 6
- مهر 1391 14
- شهریور 1391 4
- مرداد 1391 1
- تیر 1391 7
- خرداد 1391 5
- اردیبهشت 1391 6
- فروردین 1391 5
- اسفند 1390 7
- بهمن 1390 6
- دی 1390 3
- آذر 1390 15
- آبان 1390 6
- مهر 1390 6
- شهریور 1390 3
- مرداد 1390 3
- اسفند 1389 4
- بهمن 1389 5
- دی 1389 1
- مهر 1389 2
- مرداد 1389 6
- خرداد 1389 4
- اردیبهشت 1389 4
- فروردین 1389 3
- اسفند 1388 2
- بهمن 1388 2
- دی 1388 3
محاسبه آنتالپی واکنش به کمک قانون هس دقیق تره یا به کمک انتالپی های پیوند؟
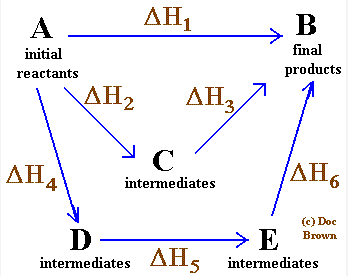
۱●دقت بالاتر دادههای ترمودینامیکی: قانون هس بر اساس دادههای ترمودینامیکی دقیق مانند آنتالپی تشکیل ترکیبات شیمیایی عمل میکند. این دادهها معمولاً از آزمایشهای دقیق و استاندارد به دست میآیند و خطای کمتری دارند. در مقابل، آنتالپی_پیوند میانگینی از انرژی پیوند در ترکیبات مختلف است و ممکن است تحت تأثیر ساختار مولکولی و محیط شیمیایی قرار گیرد، بنابراین دقت کمتری دارد.
۲● استقلال از ساختار مولکولی: - قانون هس مستقل از ساختار مولکولی است و فقط به حالت اولیه و نهایی واکنش توجه میکند. این باعث میشود محاسبات بدون در نظر گرفتن پیچیدگیهای ساختاری انجام شود. - آنتالپی پیوند به ساختار مولکولی وابسته است و ممکن است در ترکیبات مختلف متفاوت باشد، که این موضوع محاسبات را پیچیدهتر و کمتر دقیق میکند.
۳●قابلیت استفاده برای واکنشهای پیچیده: - قانون هس برای واکنشهای پیچیدهتر که شامل چندین مرحله هستند، قابل استفاده است و میتوان آنتالپی کل واکنش را با جمع جبری آنتالپی مراحل مختلف محاسبه کرد. - محاسبه آنتالپی پیوند برای واکنشهای پیچیده دشوارتر است، زیرا نیاز به در نظر گرفتن تمام پیوندهای شکسته و تشکیلشده دارد و ممکن است خطاهای بیشتری ایجاد کند.
۴● عدم نیاز به اطلاعات پیوندی: - قانون هس نیازی به اطلاعات دقیق درباره انرژی پیوندهای خاص ندارد و فقط به آنتالپی تشکیل ترکیبات شیمیایی وابسته است. - در روش آنتالپی پیوند، نیاز به دانستن انرژی تمام پیوندهای درگیر در واکنش است که ممکن است همیشه در دسترس نباشد یا دقیق نباشد.
۵● تأیید تجربی بیشتر: - قانون هس بر اساس اصول ترمودینامیکی است که به طور گسترده در آزمایشها تأیید شدهاند. این قانون به طور مستقیم از قانون اول ترمودینامیک (پایستگی انرژی) نتیجه میشود. - آنتالپی پیوند بیشتر بر اساس میانگینگیریهای تجربی است و ممکن است در شرایط مختلف نتایج متفاوتی ارائه دهد.